Antwort Wie viele Isotope hat C? Weitere Antworten – Warum ist C-12 ein Isotop
Daten und Eigenschaften des Isotops C-12.
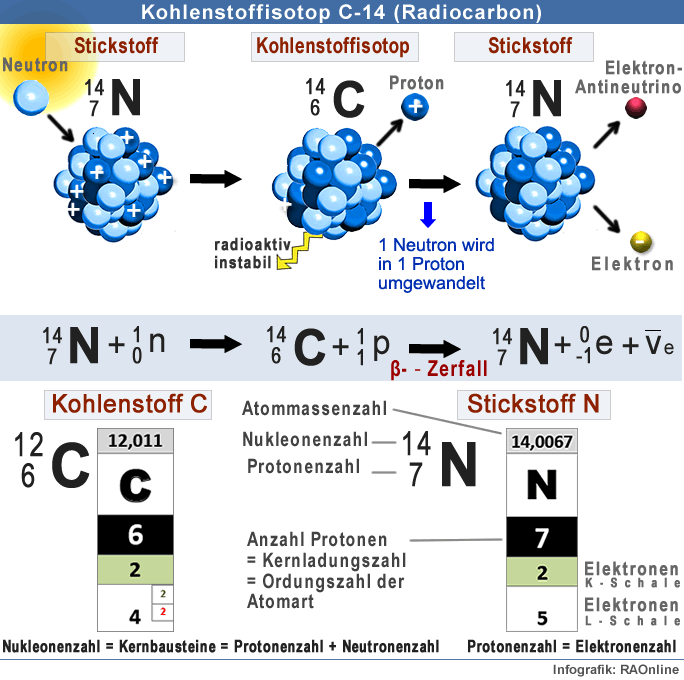
Kohlenstoff-12 ist ein stabiles Isotop des chemischen Elements Kohlenstoff, das neben den elementspezifischen 6 Protonen 6 Neutronen im Atomkern aufweist, woraus die Massenzahl 12 resultiert.In der chemischen Notation wird ein Isotop oft durch das Massenzahl-Symbol dargestellt, das oberhalb und links von dem Elementsymbol steht, zum Beispiel für Kohlenstoff-14.Arten des gleichen Atoms, die sich nur in der Anzahl der Neutronen unterscheiden, werden Isotope genannt. Die Anzahl an Protonen und die Anzahl an Neutronen zusammen bestimmen die Massenzahl: Massenzahl = Protonen + Neutronen.
Wie viele Neutronen hat ein C Atom : 6
Beispiel Kohlenstoff-Nuklid C-12: C = 6 Protonen, Massenzahl 12 minus Protonenzahl 6 = 6 Neutronen. Nuklide des gleichen chemischen Elements, also mit gleicher Protonenzahl und Ordnungszahl nennt man Isotope.
Was ist der Unterschied zwischen C 12 und C-14
Auf 1012 (1 Billion) 12C-Kerne kommt so statistisch nur ein einziger 14C-Kern. Im Gegensatz zu 12C und 13C ist 14C nicht stabil und wird deswegen auch Radiokohlenstoff genannt. Er wird allerdings auch neu gebildet.
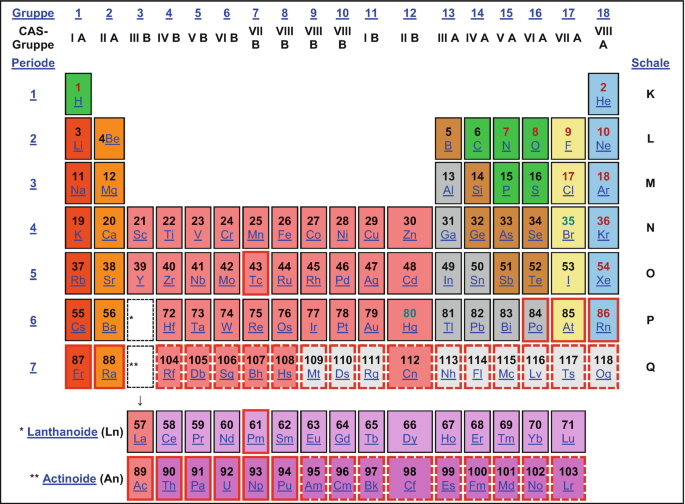
Wie viele Isotope gibt es : Bekannt sind heute knapp 300 stabile und über 2400 instabile Isotope. Jedes Element besitzt mindestens drei Isotope. Am meisten stabile Isotope hat Zinn. Am meisten Isotope überhaupt sind beim Xenon bekannt.
Isotope. Insgesamt sind 23 Isotope und zwei weitere Kernisomere zwischen 28Cl und 51Cl bekannt. Von diesen sind zwei, die Isotope 35Cl und 37Cl stabil. Natürliches Chlor besteht zu 75,77 % aus 35Cl und zu 24,23 % aus 37Cl.
Die Herstellung von Isotopen erfolgt durch den Beschuss dieser mit freien Neutronen. So entstehen etwa Uran A 92 235 A 2 92 2 235 U Isotope. Ein Uran A 92 235 A 2 92 2 235 U Isotop wird mit einem Neutron A 1 A 2 2 1 n beschossen. Dadurch entsteht ein Uran A 92 236 A 2 92 2 236 U Isotop.
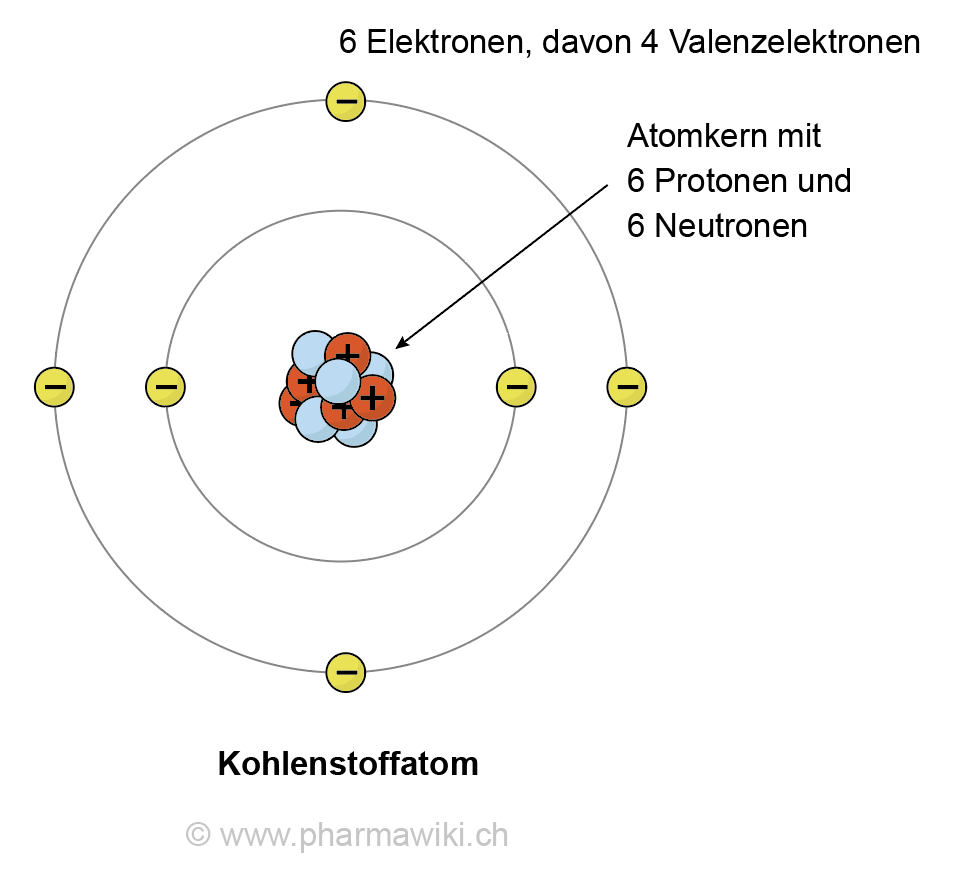
Wie viele Elektronen hat ein C Atom
2, 4Kohlenstoff / Elektronen pro SchaleDer Balken hat etwa die dreifache Länge eines Atomdurchessers. Damit ergibt sich für das Kohlenstoffatom ein Durchmesser von etwa 0,16 nm und ein Atomradius rA von 0,08 nm. In der wissenschaftlichen Literatur findet man für den Radius des Kohlenstoffatoms einen Wert von 0,076 nm.Doch 14C ist radioaktiv – eines der Neutronen im Kern wandelt sich in ein Proton um, gibt dabei ein Elektron und ein Elektron-Antineutrino ab und sendet Betastrahlung aus. Das Kohlenstoffisotop zerfällt wieder zu Stickstoff und das mit einer Halbwertszeit von 5730 Jahren.
Bis die Organismen sterben, dann nehmen sie keinen neuen Kohlenstoff, also auch kein C14 , mehr auf. Das schon vorhandene radioaktive C14 zerfällt mit einer Halbwertszeit von 5730 Jahren.
Was ist das häufigste Isotop : Das wichtigste Isotop ist dabei Protium (Wasserstoff-1 bzw. H). Es besitzt nur ein Proton und kein Neutron im Atomkern und hat eine relative Häufigkeit von 99,98 %.
Wann sind Isotope : Man spricht von Isotopen, wenn zwei Atome gleich viele Protonen haben, also dem gleichen Element angehören, aber eine unterschiedliche Zahl von Neutronen haben, also eine unterschiedliche Massenzahl aufweisen.
Haben alle Elemente Isotope
In der Regel besitzt jedes natürlich vorkommende Element ein oder wenige stabile Isotope, während seine übrigen Isotope radioaktiv (das heißt instabil) sind und früher oder später zerfallen. Es gibt jedoch auch Elemente, bei denen alle Isotope instabil sind.
Beispiele. Nehmen wir an, es handelt sich um Kohlenstoff, der sechs Protonen und sechs Neutronen, also 12 Nukleonen hat. Die erste Schreibweise ist 126C und die zweite C-12. Ein Beispiel eines besonders schweren Elements ist Uran mit 92 Protonen und 146 Neutronen, also 238 Nukleonen.Ursprung der Kohlenstoffatome
Sie ist gleich der Anzahl Protonen im Atom. 2) zu einem Kohlenstoffatom (Ordnungszahl 6). Im Kosmos ist Kohlenstoff in Bezug auf seine globale Masse das vierthäufigste Element nach Wasserstoff, Helium und Sauerstoff.
Welche Isotope hat Kohlenstoff : Kohlenstoff besitzt natürlicherweise drei Isotope: Kohlenstoff-12, Kohlenstoff-13 und Kohlenstoff-14. Mit einer Häufigkeit von 98,93 % ist dabei Kohlenstoff-12 (12C) das am häufigsten auftretende Isotop.